Efficacia e sicurezza di Lurasidone negli adolescenti con schizofrenia: uno studio di 6 settimane, randomizzato, controllato con placebo
Lurasidone al dosaggio di 40 e 80 mg/ die ha dimostrato la capacità di indurre in pazienti adolescenti con schizofrenia un miglioramento dei sintomi significativo non solo da un punto di vista statistico ma anche clinico.
Lo evidenziano i risultati dello studio multicentrico, randomizzato, in doppio cieco e controllato con placebo condotto da Robert Goldman e colleghi su un totale di 326 ragazzi di età compresa tra 13 e 17 anni con diagnosi di schizofrenia secondo il Diagnostic and Statistical Manual of Mental Disorders, 4th Edition, Text Revision (DSM-IV-TR).
La schizofrenia a insorgenza precoce (prima dei 18 anni di età) si caratterizza frequentemente per una particolare severità della sintomatologia, per l’importante impatto neurocognitivo e per una compromissione funzionale cronica, tra cui minore conseguimento di risultati scolastici, limitata capacità di condurre una vita indipendente e persistente deterioramento nel funzionamento sociale.
Da un punto di vista terapeutico, tra i farmaci antipsicotici atipici lurasidone ha dimostrato in pazienti adulti schizofrenici efficacia clinica e sicurezza sia in acuto sia sul lungo periodo, con dosaggi compresi tra 40 e 160 mg/ die (37 e 148 mg/die considerando i dosaggi europei). Questo farmaco, inoltre, ha evidenziato una scarsa propensità a indurre aumento del peso corporeo o alterazioni metaboliche.
Sulla scorta di queste osservazioni e di studi di farmacocinetica sul farmaco somministrato in età pediatrica, Goldman e colleghi hanno condotto uno studio clinico per valutare efficacia, sicurezza e tollerabilità di lurasidone in pazienti schizofrenici in età adolescenziale. I pazienti inclusi nel trial sono stati ran- domizzati in rapporto 1:1:1 a ricevere lurasidone 40 mg/die (n=108), lurasidone 80 mg/die (n=106) o placebo (n=112) per un periodo di studio di 6 settimane. Gli endpoint principali primario e secondario di efficacia erano il cambiamento dal basale alla settimana 6 nel punteggio totale al Positive and Negative Symptom Scale (PANSS) e nel punteggio Clinical Global Impressions-Severity (CGI-S), rispettivamente.
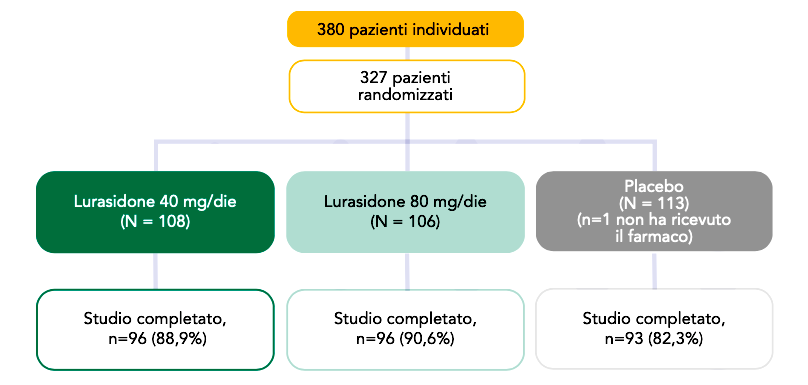
Schema di randomizzazione dei pazienti inclusi nello studio
Le valutazioni secondarie di efficacia includevano i punteggi della sottoscala PANSS (positivi, negativi, psicopatologia generale e eccitabilità), del Pediatric Quality of Life Enjoyment and Satisfaction Questionnaire (PQ-LES-Q) questionario sviluppato per aiutare nella valutazione di aspetti importanti dell’esperienza di vita nei bambini e negli adolescenti e della scala Children’s Global Assessment (CGAS) valutata dal clinico, che fornisce una misura del deterioramento funzionale.
Risultati
Il tasso di aderenza al trattamento per il periodo complessivo di studio in doppio cieco (valutato dalla conta delle compresse restituite) è stato elevato in tutti i gruppi: 100% nel gruppo lurasidone 80 mg / die, 99,0% nel gruppo lurasidone 40 mg / die e 97,3% nel gruppo placebo.
La variazione media dei minimi quadrati (LS) dal basale alla settimana 6 nel punteggio totale PANSS (endpoint primario) è stata significativamente maggiore per il gruppo lurasidone 40 mg/die (-18,6; p <0,001; dimensione dell’effetto = 0,51) e per il gruppo lurasidone 80 mg/die [-18,3; p <0,001; dimensione dell’effetto = 0,48 rispetto al gruppo placebo (-10,5)]. Entrambi i gruppi di trattamento con lurasidone 40 e 80 mg/die hanno dimostrato una separazione significativa dal placebo sul punteggio totale PANSS a partire dalla settimana 1 (p = 0,02 e p = 0,03, rispettivamente) e in tutte le visite successive.
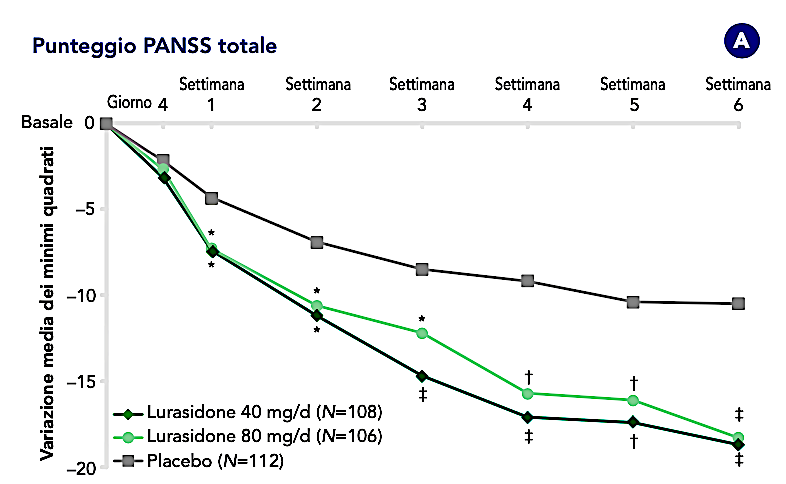
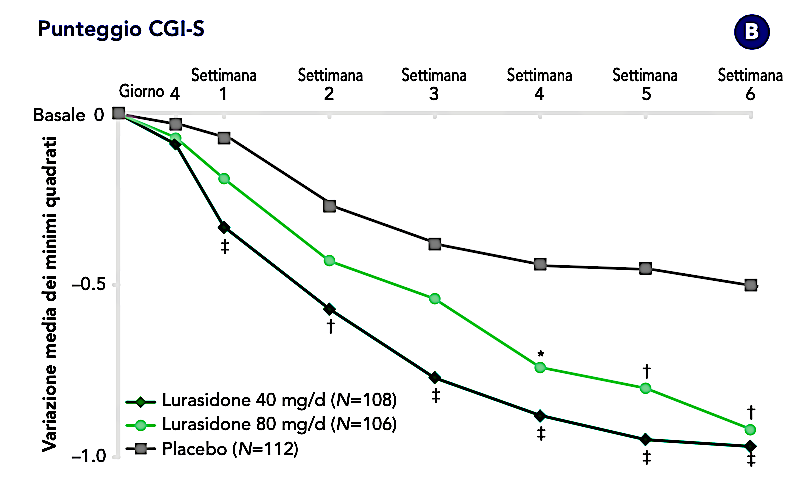
Variazione media dei minimi quadrati in (A) punteggio totale PANSS e (B) punteggio CGI-S dal basale fino alla settimana 6 negli adolescenti con schizofrenia trattati con lurasidone 40 mg/die, lurasidone 80 mg/die o placebo (analisi MMRM, popolazione ITT). * p <0,05; † p <0,01; ‡ p <0,001 rispetto al placebo. CGI-S, Clinical Global Impressions-Severity; ITT, intent-to-treat; MMRM, mixed model for repeated measurement; PANSS, Positive and Negative Syndrome Scale; SD, deviazione standard.
ll miglioramento del punteggio totale PANSS dal basale alla settimana 6 (LOCF) è stato simile nei pazienti di età compresa tra 13 e 15 anni (variazione media LS di -18,0 nel gruppo lurasidone 40 mg/ die, -17,8 nel gruppo lurasidone 80 mg/die e -10,1 nel gruppo placebo) e nei pazienti di età compresa tra 16 e 17 anni (variazione media LS di -16,2 nel gruppo lurasidone 40 mg/die, -15,7 nel gruppo lurasidone 80 mg/die e -7,7 nel gruppo placebo).
La variazione media LS dal basale alla settimana 6 nel punteggio CGI-S (endpoint secondario chiave) è stata significativamente maggiore per il gruppo lurasidone 40 mg/die (-1,0; p <0,001; dimensione dell’effetto = 0,49) e lurasidone 80 mg/die gruppo (-0,9; p = 0,0015; dimensione dell’effetto = 0,45) rispetto al gruppo placebo (-0,5). Entrambi i gruppi di trattamento con lurasidone hanno dimostrato un miglioramento significativo rispetto al placebo nelle sottoscale PANSS, nel PQ-LES-Q e nella CGAS valutata dal clinico.
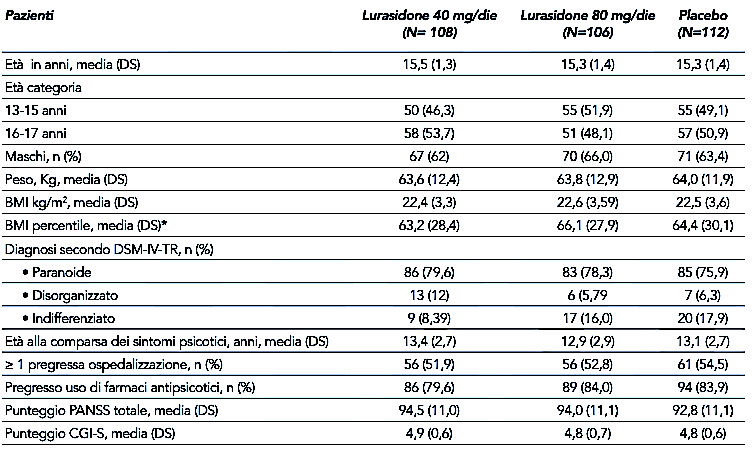
Caratteristiche demografiche e cliniche al basale degli adolescenti con schizofrenia (popolazione intent-to-treat).
* Secondo le tavole di crescita di riferimento dell'Organizzazione mondiale della sanità 2007.
BMI, body mass index; CGI-S, Clinical Global Impressions-Severity; DSM-IV-TR, Diagnostic and Statistical Manual of Mental Disorders, 4° Edizione, Text Revision; PANSS, Positive and Negative Syndrome Scale; DS, deviazione standard.
Non sono state rilevate differenze di trattamento clinicamente significative tra i gruppi lurasidone e placebo sulle misurazioni di laboratorio dei parametri lipidici, degli indici glicemici e dei livelli di prolattina. La maggior parte degli eventi avversi (principalmente rappresentati da nausea, acatisia e sonnolenza) è stata segnalata come di gravità lieve o moderata ed era coerente con il profilo di sicurezza di lurasidone riscontrato negli adulti. Meno del 3% dei pazienti adolescenti trattati con lurasidone ha riportato eventi classificati come gravi, percentuale comparabile con l’incidenza riportata nel gruppo placebo.
Conclusioni
In questo studio di efficacia e sicurezza di 6 settimane controllato con placebo, lurasidone a dosi fisse di 40 e 80 mg / die ha fornito un miglioramento dei sintomi statisticamente significativo e clinicamente significativo nei pazienti adolescenti con schizofrenia. Sono stati anche osservati miglioramenti significativi nelle capacità funzionali e nella qualità della vita. Lurasidone è stato generalmente ben tollerato e ha avuto pochi effetti sul peso, sui parametri metabolici e sulla prolattina, simili ai dati di sicurezza nei pazienti adulti con schizofrenia.
Key Points dello studio
1- La schizofrenia a insorgenza precoce (<18 anni di età) è frequentemente caratterizzata da:
- severità della sintomatologia
- impatto neurocognitivo
- compromissione funzionale cronica (difficoltà scolastiche e nella vita di relazione)
2 - Lurasidone, farmaco antipsicotico atipico, ha indotto a dosi fisse di 40 e 80 mg/die (37 e 74 mg secondo i dosaggi europei) un miglioramento dei sintomi statisticamente e clinicamente significativo nei pazienti adolescenti (età 13-17 anni) con schizofrenia.
3 - Lurasidone ha prodotto miglioramenti significativi anche sulla qualità della vita e nelle capacità funzionali.
4 - Lurasidone si è dimostrato ben tollerato negli adolescenti con pochi effetti sul peso, sui parametri metabolici e sulla prolattina, con un profilo di sicurezza simile a quello dei pazienti adulti con schizofrenia.
5 - Il tasso di aderenza al trattamento con lurasidone negli adolescenti è risultato elevato con percentuali del 100% e 99% con i dosaggi rispettivamente di 80 e 40 mg/die (37 e 74 mg secondo i dosaggi europei)
Lurasidone è indicato per il trattamento della schizofrenia negli adulti e negli adolescenti a partire dai 13 anni di età (Riassunto delle caratteristiche del prodotto).
Bibliografia Robert Goldman, Antony Loebel, Josephine Cucchiaro, Ling Deng, Robert L. Findling. Journal of Child and Adolescent Psychopharmacology 2017 Volume 27, Number 6, 516–525
Commenti
Lascia un commento:

Clinical Practice è un sito del network XGATE
XGate è un sistema di registrazione centralizzato che permette di accedere con le stesse credenziali (Email e password) a tutti i siti e app realizzati da Axenso



