
Elio M. Staffiere
Responsabile Servizio di Cardiologia dell’Istituto Suore Cappuccine di Madre Rubatto di Bergamo
Fattori di rischio cardiovascolari classici ed emergenti: A(P)PUNTI di pratica clinica
Elio M. Staffiere
Responsabile Servizio di Cardiologia dell’Istituto Suore Cappuccine di Madre Rubatto di Bergamo
“I sani sono malati che non sanno di esserlo” J. Romain
Secondo l’Organizzazione Mondiale della Sanità la salute è “uno stato di benessere fisico, psicologico e sociale completo”. Possiamo dedurre che a star bene nel mondo siano pochi privilegiati e per costoro è comunque una condizione momentanea.
Per migliorare lo stato di salute servono conoscenza dei fattori di rischio e capacità di autocontrollo. Per ottenere buoni risultati in questo campo è necessario sfoderare “l’arte medica” che è sintesi tra fiducia, coscienza e sapere e richiede una visione non riduttiva e nozionistica della medicina.
La medicina ha sempre cercato di dare una rappresentazione scientifica al rapporto tra emozioni, salute e malattia, di saper leggere la “grande connessione” tra cuore e mente, “tra l’organo che c’è e l’organo che non c’è”.
Un potente aiuto per poter interpretare questi fini meccanismi arriva dalle neuroscienze che negli ultimi anni hanno fornito ampie conoscenze in materia.
Le neuroscienze ci hanno permesso di fare un grosso salto nel futuro sovvertendo il credo culturale che “nella scienza i sentimenti non contano” e dimostrando come, attraverso un complesso dialogo di sistema che vede coinvolte anche le emozioni, sostanze come neuropeptidi, citochine, fibre nervose periferiche e sistema immunitario siano in grado di creare una rete, un network di medicina integrata, capace di controllare l’equilibrio dinamico dell’organismo umano.
Il sintomo o la malattia rappresentano un momentaneo disequilibrio di questo network.
Attraverso questo testo abbiamo cercato di tradurre tutto ciò in “A(P)PUNTI” al fine di fornire informazioni agili e speriamo utili per il vostro lavoro.
I fattori di rischio classici "non modificabili" e modificabili"
Le malattie cardiovascolari rappresentano ancora la principale causa di morte nel nostro Paese con il 44% tra tutti i decessi. La cardiopatia ischemica è la prima causa di morte in Italia con una percentuale del 28%; mentre gli accidenti cerebrovascolari sono al terzo posto con il 13%, dopo i tumori. Le malattie cardiovascolari modificano la qualità di vita dei pazienti e comportano notevoli costi economici per la società.
In Italia la prevalenza di cittadini affetti da invalidità cardiovascolare è pari al 4,4 per mille (dati Istat). Il 23,5% della spesa farmaceutica italiana (pari all'1,34 del prodotto interno lordo), è destinata a farmaci per il sistema cardiovascolare.1
Le malattie cardiovascolari (CVD) sono caratterizzate da una serie di disturbi che interessano il cuore e i vasi sanguigni e comprendono:2
- Malattia coronarica;
- Malattia cerebrovascolare;
- Malattia arteriosa periferica;
- Cardiopatia reumatica;
- Cardiopatia congenita;
- Trombosi venosa profonda ed embolia polmonare.
L'industrializzazione dell'economia con un conseguente passaggio da lavori fisicamente impegnativi a lavori sedentari, insieme all'attuale consumismo e cultura guidata dalla tecnologia che è correlata a orari di lavoro più lunghi, spostamenti più frequenti e duraturi, e meno tempo libero per attività ricreative, può spiegare il significativo e costante aumento dei tassi di malattie cardiovascolari (CVD) negli ultimi decenni. In particolare, l'inattività fisica, l'assunzione di una dieta ipercalorica, i grassi saturi e gli zuccheri sono associati allo sviluppo di aterosclerosi e altri disturbi metabolici come la sindrome metabolica, il diabete mellito e l'ipertensione che sono altamente prevalenti nelle persone con CVD.2
Nell’ambito cardiovascolare esistono alcuni fattori di rischio che aumentano la probabilità di eventi cardiaci. Tali fattori comprendono tutte quelle condizioni che aumentano la probabilità di ammalarsi di una malattia del cuore e dei vasi.
I fattori di rischio possono essere classificati in modificabili (fumo, ipertensione arteriosa, ipercolesterolemia, basso colesterolo HDL, diabete, eccessivo consumo di alcool, dieta ricca di grassi e ipercalorica, ridotta attività fisica) e non modificabili (sesso, età, familiarità, storia di malattia cardiovascolare pregressa).3
I fattori di rischio classici "non modificabili"
Età
”Il segreto è arrivare a 80 anni. Dopo è una passeggiata” - Dino Risi
Il maggiore indicatore dello stato di salute cardiovascolare di un individuo è l'età. Si stima che entro il 2030, circa il 20% della popolazione avrà un’età ≥ 65 anni e le malattie cardiovascolari incideranno su circa il 40% dei decessi inerenti a questa fascia di età.4
Con l’avanzare dell’età, si verificano cambiamenti importanti a livello cardiovascolare anche in soggetti sani, come l’ispessimento e l'irrigidimento delle grandi arterie causato dai depositi di collagene e calcio e dalla perdita di fibre elastiche nello strato mediale. Questi cambiamenti arteriosi provocano un aumento della pressione sistolica in soggetti più anziani, mentre la pressione diastolica generalmente diminuisce dopo i 60 anni.5
L'elevata incidenza di eventi cardiovascolari nella popolazione anziana è stata associata ad una serie di fattori, tra cui l’aumento dello stress ossidativo, una maggiore condizione infiammatoria, apoptosi e un deterioramento miocardico in generale. Inoltre, è risaputo che un aumento della produzione delle specie reattive dell’ossigeno (ROS) si verifica con l’avanzare dell’età. Tale condizione è stata associata ad una condizione di infiammazione persistente e ad una cronicità, tipica delle malattie cardiovascolari.6
L'età avanzata è stata definita da una serie di punteggi di rischio cardiovascolari come il fattore di rischio cardiovascolare più impattante.
Con il passare degli anni assistiamo ad un aumento dei fattori di rischio cardiovascolari. Tuttavia, un’analisi di regressione multivariata ha dimostrato come l'età rappresenta un fattore di rischio cardiovascolare indipendente.7
Genere
“Arricchiamoci delle nostre reciproche differenze” Paul Valéry
Sebbene l'età sia un fattore di rischio indipendente per le malattie cardiovascolari, è evidente che le donne anziane siano più inclini a determinate complicazioni correlate alle malattie cardiache. Generalmente, prima della menopausa, le donne sono relativamente protette dalle malattie cardiovascolari mentre subito dopo la menopausa, il rischio di malattie cardiache aumenta notevolmente.6
Rispetto alla popolazione maschile, le malattie cardiovascolari nelle donne si manifestano con un ritardo che va dai 7 ai 10 anni.9
Si presume che l'esposizione agli estrogeni endogeni durante il periodo fertile ritardi la manifestazione della malattia aterosclerotica nelle donne. Prima della menopausa, il tasso di eventi associati alla sindrome coronarica nelle donne è basso e prevalentemente attribuito al fumo. Le donne con malattia coronarica (CHD) sono generalmente più anziane degli uomini, con una maggiore espressione di fattori di rischio cardiovascolare. Sebbene donne e uomini condividano i fattori di rischio più classici, il valore e il peso relativo di questi fattori sono diversi. In età più giovane (9
Durante l'invecchiamento, la pressione sistolica aumenta più rapidamente nelle donne rispetto agli uomini e questo può essere correlato alla riduzione dei livelli di estrogeni durante la menopausa. In età avanzata (> 75 anni) l'ipertensione sistolica isolata è più diffusa nelle donne ed è un'importante causa di ipertrofia ventricolare sinistra, insufficienza cardiaca (diastolica) e ictus. L'ipertensione moderata o borderline (9
In giovane età, il rischio relativo di ipercolesterolemia è inferiore nelle donne rispetto agli uomini. Durante la menopausa, i livelli di colesterolo totale e delle lipoproteine a bassa densità (LDL) aumentano rispettivamente del 10 e del 14% e la lipoproteina (a) aumenta dal 4 all'8%, mentre i livelli di colesterolo delle lipoproteine ad alta densità (HDL) rimangono invariati.9
Sebbene gli studi abbiano dimostrato che la disfunzione ormonale nelle donne in premenopausa è associata ad un aumentato rischio di aterosclerosi e di eventi CHD, non è ancora chiaro se la sindrome dell'ovaio policistico (PCOS) sia un fattore di rischio indipendente per l'aterosclerosi. Le donne con questa sindrome sono a maggior rischio di sviluppare la sindrome metabolica e il diabete mellito di tipo 2. 9
Familiarità
“La migliore prevenzione cardiovascolare stà nello scegliersi i giusti genitori” - E. Braunwald
La familiarità per eventi cardiovascolari è definita dalla presenza di almeno un parente di primo grado di sesso maschile (età 29
Un'elevata prevalenza di malattie cardiovascolari all'interno di una famiglia può indicare fattori ambientali, culturali e comportamentali condivisi e in precedenza si pensava che la presenza di questi fattori di rischio sopra menzionati spiegasse in gran parte l'aggregazione di una determinata malattia cardiovascolare in alcune famiglie. Ad esempio, fattori di rischio ambientale condivisi, come la presenza di fumo e una dieta non salutare, rappresentano alcuni dei maggiori rischi di CVD nella prole con genitori affetti. 20
Tuttavia, è stato dimostrato che la storia famigliare di malattia coronarica fosse associata ad un maggior rischio di sviluppare un infarto al miocardio indipendentemente dalla presenza di altri fattori di rischio. 20
Inoltre, i fattori genetici coinvolti nella gestione dell'equilibrio delle lipoproteine, nell'integrità endoteliale, nell'infiammazione arteriosa e nella formazione di trombosi sono stati associati ad un aumento del rischio di CVD in famiglia.20
I fattori di rischio classici "non modificabili" in A(P)PUNTI



I fattori di rischio classici "modificabili"
Fumo
“Smettere di fumare è facilissimo. Io ci sono riuscito almeno mille volte” - M. Twain
Il fumo è la più importante causa di morte prevenibile nel mondo occidentale e ogni anno causa circa 5 milioni di morti premature. Il fumo di sigaretta è un importante fattore di rischio per le malattie cardiovascolari (CVD) e la seconda causa di mortalità per CVD dopo l’ipertensione. Le malattie cardiovascolari sono responsabili di > 17 milioni di decessi in tutto il mondo ogni anno, di cui si stima che oltre il 10% sia causato dal fumo di sigaretta.23
Obesità
“Gli obesi vivono di meno però mangiano di più” - Anonimo
L'eccesso di peso corporeo è un importante fattore di rischio di mortalità e di morbidità da malattie cardiovascolari, che causa quasi 3 milioni di decessi all'anno in tutto il mondo.27
Nel 1998 una Task Force della AACE/American College of Endocrinology Obesity ha definito l’obesità come “…una condizione complessa e multifattoriale caratterizzata da un eccesso di grasso corporeo. Deve essere considerato come un disturbo cronico che richiede essenzialmente cure, supporto e follow-up continui. L'obesità causa molte altre malattie….”.28
Le maggiori complicanze cliniche associate ad un aumento del peso corporeo sono rappresentate
da ipertensione arteriosa, dislipidemie, insulino-resistenza, processi infiammatori e protrombotici, albuminuria e insorgenza di diabete mellito (DM) ed eventi CV (SC, CAD, FA e ictus).22
Secondo i dati del NHANES III, tra gli uomini, la prevalenza di soggetti con pressione elevata aumenta progressivamente con l’aumento dell’indice di massa corporea (BMI), con il 15% per BMI 2 e il 42% per BMI > 30 kg/m2.29
Ipertensione arteriosa
”Non conoscere la propria pressione sanguigna, è come non conoscere il valore della propria azienda” - Mehmet Oz
L'ipertensione è uno dei più importanti fattori di rischio per le malattie cardiovascolari (CVD), e rappresenta la principale causa di morte. Circa il 54% degli ictus e il 47% delle malattie coronariche, in tutto il mondo, sono attribuibili ad una pressione arteriosa elevata. L'ipertensione è una condizione comune. La sua prevalenza aumenta con l'età e si stima che colpisca il 65% dei 60enni. La popolazione mondiale sta invecchiando. Entro il 2030, circa il 20% della popolazione mondiale avrà 65 anni. Pertanto, si prevede che l'impatto dell'elevata pressione arteriosa sulla mortalità tra gli anziani aumenterà nei prossimi decenni.32
Dislipidemie
È meglio amare o essere amati? Nessuno dei due se il vostro colesterolo è più di seicento. Woody Allen
Il ruolo cruciale della dislipidemia, in particolare dell'ipercolesterolemia, nello sviluppo di CVD è documentato oltre ogni dubbio da studi genetici, patologici, osservazionali e interventistici.36
Esiste un'associazione positiva forte e graduale tra il colesterolo presente nelle C-LDL e quello totale e il rischio di CVD. Questa associazione si applica a uomini e donne sia con CVD conclamata che in assenza di CVD. L'evidenza che la riduzione dei livelli plasmatici di C-LDL riduce il rischio di CVD è inequivocabile; i risultati di studi epidemiologici e delle sperimentazioni con endpoint angiografici o clinici confermano che la riduzione del colesterolo LDL è di primaria importanza nella prevenzione della CVD.36
Diverse metanalisi mostrano una riduzione relativa dose-dipendente di CVD con l'abbassamento dei livelli di C-LDL. Una riduzione di 1,0 mmol / L di C-LDL è associata a una riduzione del 20-25% del tasso di mortalità per CVD e IM non fatale.36
L'ipertrigliceridemia è un fattore di rischio cardiovascolare indipendente significativo, ma l'associazione è molto più debole rispetto all'ipercolesterolemia. Il rischio è associato più fortemente all'ipertrigliceridemia moderata rispetto a quella molto grave [>10 mmol / L (> ~ 900 mg / dL)], un fattore di rischio per la pancreatite. Diverse meta-analisi suggeriscono che il targeting dei trigliceridi può ridurre la CVD in sottogruppi specifici con trigliceridi alti e basso C-HDL. Al momento, livelli di trigliceridi a digiuno > 1,7 mmol / L (> ~ 150 mg / dL) continuano ad essere considerati un marker di aumento del rischio, ma le concentrazioni ≤1,7 mmol / L non sono livelli target basati sull'evidenza per la terapia. 36
Bassi livelli di C-HDL risultano indipendentemente associati ad un maggiore rischio di CVD. Inoltre, valori minimi di C-HDL sono assieme all'ipercolesterolemia un fattore di rischio per la malattia coronarica. Livelli di trigligeridi moderatamente elevati e basse concentrazioni di C-HLD sono molto comuni tra i pazienti diabetici di tipo 2, con obesità addominale e tra i pazienti resistenti all'insulina. L'attività fisica e altri fattori dello stile di vita, piuttosto che il trattamento farmacologico, rimangono mezzi importanti per aumentare i livelli di C-HDL. 36
Le recenti Linee Guida internazionali sulla gestione delle dislipidemie prodotte dall’European Society of Cardiology(ESC) e dall’European Atherosclerosis Society (EAS) del 2019 suggeriscono nuovi target di trattamento.37
Il primo obiettivo è stratificare correttamente la categoria di rischio mediante le carte SCORE. Sulla base del dato ottenuto si proporranno nuovi target di trattamento qui sotto riportati in sintesi:37
- Pazienti a rischio molto alto (rischio di morte cardiovascolare a 10 anni ≥ 10%): ridurre il colesterolo LDL di almeno il 50% rispetto ai livelli basali e al di sotto dei 55 mg/dl;
- Pazienti a rischio molto alto che manifestano un secondo evento vascolare (non necessariamente uguale) entro 2 anni dal primo durante terapia con statine al dosaggio maggiore tollerabile: ridurre il colesterolo LDL sotto i 40 mg/dl;
- Pazienti a rischio alto (rischio di morte cardiovascolare a 10 anni ≥ 5% – < 10%): ridurre di almeno il 50% i valori di colesterolo LDL rispetto a quelli iniziali e < 70 mg/dl;
- Pazienti a rischio moderato (rischio di morte cardiovascolare a 10 anni ≥ 1% – < 5%): ridurre il colesterolo LDL sotto i 100 mg/dl;
- Pazienti a rischio basso (rischio di morte cardiovascolare a 10 anni < 1%): ridurre il colesterolo LDL sotto i 116 mg/dl.
- Tra le popolazioni speciali, il trattamento con statine è raccomandato nei soggetti con età inferiore ai 75 anni in prevenzione primaria; per soggetti con età superiore ai 75 anni l’introduzione della statina va considerata se presente rischio CV almeno alto.
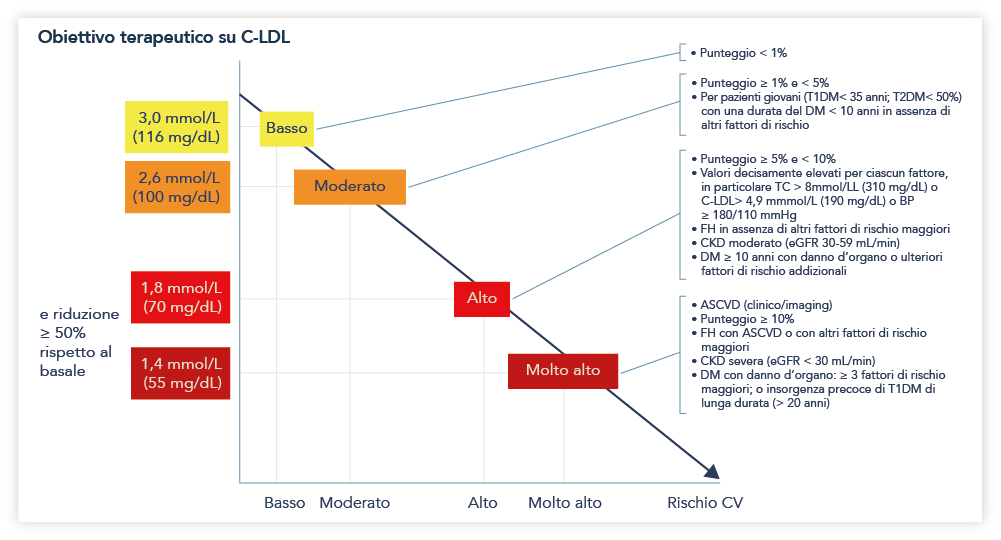
Figura 1. Obiettivi del trattamento per il colesterolo lipoproteico a bassa densità tra le categorie di rischio di malattie cardiovascolari totali.
Tratta da Figura 4 di ref. 37.
ASCVD = malattia cardiovascolare aterosclerotica; BP = pressione sanguigna; CKD = malattia renale cronica; CV = cardiovascolare; DM = diabete mellito; eGFR = velocità di filtrazione glomerulare stimata; FH = ipercolesterolemia familiare; LDL-C = colesterolo lipoproteico a bassa densità; PCSK9 = proproteina convertasi subtilisina / kexina tipo 9; SCORE = punteggio del rischio cardiovascolare; T1DM = diabete di tipo 1; T2DM = diabete di tipo 2; TC = colesterolo totale.
Diabete
“Lei era talmente dolce che a lui venne il diabete” - E. Drusiani
Entro il 2030, le persone affette da diabete mellito (DM) saranno circa 550 milioni. Tuttavia, si stima che questo numero potrebbe essere anche superiore.
Nonostante i vantaggi significativi nelle strategie di gestione che riducono i fattori di rischio di CVD aterosclerotichi (ASCVD), la CVD è rimasta la principale causa di morbilità e mortalità nei pazienti con diabete di tipo 2 (T2DM). La buona notizia è che gli esiti letali delle malattie cardiovascolari sono diminuiti in modo significativo sia in T1DM che in T2DM tra il 1998 e il 2014. Il diabete mellito è un fattore di rischio indipendente di CVD ed è associato a un rischio più elevato di CVD maggiore nella popolazione femminile.37
Dati recenti indicano che il DM di per sé aumenta il rischio di CVD in media circa due volte, ma il rischio è soggetto ad ampie variazioni a seconda della popolazione e alla terapia profilattica corrente. È importante sottolineare che pazienti affetti da DM e CAD hanno un rischio di CVD sostanzialmente più elevato. Nel T2DM, il rischio di ASCVD è fortemente determinato dalla presenza di danno d'organo bersaglio - inclusa nefropatia (microalbuminuria), neuropatia o retinopatia - con i rischi che aumentano in relazione al numero di condizioni presenti. Ipertensione, dislipidemia, obesità addominale e steatosi epatica non alcolica (NAFLD) coesistono comunemente con T2DM e aggravano ulteriormente il rischio, che è più alto nelle persone con T2DM e fattori di rischio cardiometabolici multipli. È importante sottolineare che il DM conferisce un rischio di mortalità in eccesso a seguito all'insorgenza della Sindrome coronarica acuta, evidenziando la prognosi infausta dei pazienti coronarici con T2DM e la necessità di una terapia intensiva. Come catturare il rischio extra oltre i tradizionali fattori di rischio nella pratica clinica è una questione dibattuta. Un approccio pratico è che se si identifica un componente, si dovrebbe fare una ricerca sistematica per gli altri.37
Aderenza teraputica
“Nessun uomo di buon senso può credere nelle medicine per malattie croniche” - G. Meredith
L’aderenza terapeutica può essere definita come “il coinvolgimento attivo, volontario e collaborativo del paziente, finalizzato a produrre un risultato terapeutico”.41
Aderenza terapeutica in soggetti ad alto rischio e in pazienti con CVD è bassa, con conseguenti esiti peggiori e costi sanitari più elevati.36
Un mese dopo ad un evento di infarto al miocardio acuto, il 25-30% dei pazienti interrompe la terapia, e l'aderenza alla terapia si riduce progressivamente nel tempo. Dopo 1 anno, solo il 50% dei pazienti riferisce un uso persistente della terapia. Le ragioni della scarsa aderenza sono multifattoriali.36
La mancata aderenza terapeutica correlata ai costi sanitari è un problema rilevante in molti Paesi. La depressione raddoppia in maniera indipendente il rischio di mancata aderenza al trattamento.36
Nella pratica clinica, i medici dovrebbero valutare l'aderenza al farmaco, identificare i motivi della possibile scarsa o mancata aderenza e promuovere l'aderenza secondo i seguenti principi stabiliti:36
- Fornire informazioni chiare sui benefici e sui possibili effetti collaterali della terapia, nonché sulla sua durata e sui tempi di assunzione;
- Tenere in considerazione le abitudini e le preferenze del paziente (prendere decisioni condivise);
- Semplificare quanto più possibile lo schema di assunzione della terapia;
- Domandare al paziente in maniera non inquisitoria come funziona la terapia e valutare insieme i possibili motivi di non aderenza (es. effetti collaterali, preoccupazioni);
- Attuare un costante monitoraggio con feedback del paziente;
- Far intervenire un assistente e/o un infermiere qualificato o un farmacista ogniqualvolta sia necessario e possibile;
- In caso di persistente non aderenza terapeutica, proporre interventi comportamentali combinati o multisessione (es. in ambito di riabilitazione cardiaca [RC] dopo un intervento di rivascolarizzazione miocardica).
Sedentarietà
“Il moto è la migliore cura della malinconia” - Bruce Chatwin
Una regolare attività fisica comporta una diminuzione del rischio di numerosi eventi avversi in tutte le fasce di età, con una riduzione della mortalità per ogni causa e CV negli individui sani (pari al 20-30% con una relazione dose-risposta, nei soggetti con fattori di rischio coronarico che nei pazienti con cardiopatie.22
L’attività fisica esercita effetti positivi su molti fattori di rischio, quali ipertensione arteriosa, colesterolo legato alle lipoproteine a bassa densità (C-LDL), colesterolo non-HDL, peso corporeo e DM di tipo 2. Tali effetti si esplicano tanto negli uomini quanto nelle donne e per tutte le fasce di età dall’infanzia alla senilità. Uno stile di vita sedentario rappresenta uno dei maggiori fattori di rischio per MCV indipendentemente dal praticare o meno attività fisica.22
L’attività fisica maggiormente studiata e raccomandata è quella di tipo aerobico, caratterizzata da una favorevole relazione dose-risposta in termini di miglioramento della prognosi.22
I fattori di rischio classici "modificabili" in A(P)PUNTI







Prevenzione cardiovascolare con antiaggreganti
La prevenzione cardiovascolare può essere realizzata anche con farmaci che non correggono direttamente un fattore di rischio specifico, il cui effetto è meno facilmente misurabile, gli antiaggreganti. piastrinici*.
Il loro meccanismo d’azione come noto è legato alla soppressione dell’aggregazione delle piastrine, situazione tanto più importante e determinante nella protezione del paziente, quanto maggiore è il livello di rischio del soggetto.46
Diamo quindi per scontato il ruolo riconosciuto universalmente all’ASA di caposaldo nel paziente con pregresso evento cardiovascolare maggiore o malattia aterosclerotica sintomatica. 46
In questa sessione invece ci occupiamo soprattutto della cosiddetta prevenzione primaria, quella che si realizza nei soggetti che non hanno avuto un evento CV maggiore.
Va subito chiarito, di fronte alla estrema eterogenicità dei soggetti in prevenzione primaria, il nostro interesse si deve concentrare su quelli che hanno comunque un rischio cardiovascolare elevato. Solo in pazienti con un profilo di rischio elevato infatti ha una valenza clinica l’utilizzo di antiaggreganti, l’acido-acetilsalicilico in primis.46
Riassumiamo molto schematicamente, come A(P)PUNTI, le situazioni più comuni in cui l’uso di l’acido-acetilsalicilico è raccomandato e/o suggerito in prevenzione primaria dagli enti regolatori e dai documenti di consenso:
- Soggetti ad elevato rischio CV, con un livello di rischio di incorrere in un serio evento cv >20% a 10 anni; misurazione con le C. del Rischio Progetto Cuore 15
- Soggetti a rischio CV intermedio senza aumentato rischio di sanguinamento e familiarità per i tumori del tratto gastro-intestinale (cancro colo-rettale in primis), sebbene in Italia non è indicato per questa tipologia di pazienti.46 (Figura 2)
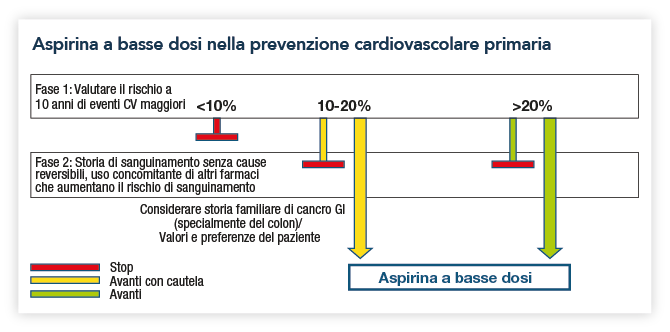
Fig. 2 - Algoritmo pratico proposto dal ESC Working Group on Thrombosis e ripreso dal Documento di Consenso Intersocietario Italiano sull'utilizzo di aspirina in prevenzione Cv primaria
- Soggetti diabetici, purché a rischio cardiovascolare alto.
Oggi le principali linee guida sottolineano l’infelice condizione del diabetico dal punto di vista del rischio CV.
Le recenti Linee guida ESC-EASD 2019 definiscono ad alto rischio un soggetto con DM ll da almeno 10 anni più un fattore di rischio cv addizionale (ipercolesterolemia, ipertensione, familiarità per evento CV).40 (Figura 3).Le Linee Guida Europee della Società di Cardiologia e del Diabete raccomandano, quando necessario l’utilizzo di PPIs per prevenire i sanguinamenti gastro-intestinali, permettendo una migliore aderenza e persistenza alla terapia.40
Analogamente quelle dell’American Diabetes Association del 2020 suggeriscono, con un grado di evidenza A, l’uso di ASA a basse dosi nei soggetti diabetici over 50 con un fattore di rischio addizionale.47

Fig. 3 - Tratto dalle Linee guida ESC-EASD 2019.40
DM = diabete mellito. a: Modificato dalle Linee Guida Europee 2016 sulla prevenzione della malattia cardiovascolare nella pratica clinica. b: Proteinuria, insufficienza renale definita come eGFR ≥ 30 mL/min/1.73 m2, ipertrofia ventricolare sinistra, o retinopatia. c: Età, ipertensione, dislipidemia, fumo, obesità.
Conclusioni
Parlando della prevenzione con ASA, unico antiaggregante approvato per la prevenzione primaria, il mio consiglio è quella di analizzare il livello del rischio del soggetto, usando le carte del rischio, ricercando condizioni che aumentano la possibilità di andare incontro ad un evento cardio-cerebrovascolare tenendo presente il rischio di emorragie ed eventuali strategie per prevenirle laddove possibile (esempio: l’uso di PPIs). 40,46
Inoltre, possono essere presi in considerazione effetti preventivi oncologici (presenti peraltro tra le proprietà farmacodinamiche in scheda tecnica) che potrebbero supportare una migliore aderenza nel paziente cardiovascolare.15
BIBLIOGRAFIA
- https://www.epicentro.iss.it/cardiovascolare/
- Lopez et al. Cardiovascular Disease. StatPearls - NCBI Bookshelf.
- Brown et al. Risk Factors For Coronary Artery Disease. StatPearls - NCBI Bookshelf
- North BJ and Sinclair DA. The Intersection Between Aging and Cardiovascular Disease. Circ Res. 2012 April 13; 110(8): 1097–1108.
- Fleg JL. Age-associated changes in cardiovascular structure and function: a fertile milieu for future disease. Heart Fail Rev. 2012 September; 17(0): 545–554.
- Rodgers JL et al. Cardiovascular Risks Associated with Gender and Aging. J. Cardiovasc. Dev. Dis. 2019, 6, 19.
- Dhingra R. et al. Age as a Cardiovascular Risk Factor. Med Clin North Am. 2012; 96(1): 87–91
- Patti G et al. Thromboembolic Risk, Bleeding Outcomes and Effect of Different Antithrombotic Strategies in Very Elderly Patients With Atrial Fibrillation: A Sub-Analysis From the PREFER in AF (PREvention oF Thromboembolic Events–European Registry in Atrial Fibrillation). J Am Heart Assoc. 2017;6:e005657
- Maas AHEM and Appelman YEA. Gender differences in coronary heart disease. Neth Heart J. 2010; 18(12): 598–602
- https://www.who.int/data/gho/data/themes/theme-details/GHO/women-and-health
- Cardiovascular Disability: Updating the Social Security Listings. Washington (DC): National Academies Press (US); 2010
- The WHO CVD Risk Chart Working Group. World Health Organization cardiovascular disease risk charts: revised models to estimate risk in 21 global regions. Lancet Glob Health 2019; 7: e1332–45
- Garcia M et al. Cardiovascular Disease in Women: Clinical Perspectives. Circ Res. 2016 April 15; 118(8): 1273–1293.
- Fang M et al. Gender Differences in the Risk of Ischemic Stroke and Peripheral Embolism in Atrial Fibrillation: The AnTicoagulation and Risk factors In Atrial fibrillation (ATRIA) Study. Circulation. 2005 September 20; 112(12): 1687–1691.
- Cardioaspirin 100 mg RCP di prodotto.
- Whang W et al – Depression e risk of sudden cardiac death and coronary heart disease in women: results froNurses’ Health Study. J Am Coll Cardiol 2009; 53:950-958.
- Templin C et al – Clinical Features and Outcomes of Tako-Tsubo (Stress) cardiomiopathy – NEJM 2015:373;929-938.
- Edwards FH et al – Impact og gender on coronary bypass operative mortality. Ann Thorac Surg 1998; 66:125-31
- Red Alert for Women’s Heart. Woman and Cardiovascular research in Europe – 2009.
- Allport SA et al. Parental Age of Onset of Cardiovascular Disease as a Predictor for Offspring Age of Onset of Cardiovascular Disease. PLoS One. 2016; 11(12): e0163334.
- Bechmann JM et al – Association between family history and coronary heart disease death across long-term follow-up in men: the CooperCenter Longitudinal Study. Circulation 2012;125:3092-3098
- Piepoli MF et al. Linee guida europee 2016 sulla prevenzione delle malattie cardiovascolari nella pratica clinica. G Ital Cardiol 2017;18(7-8):547-612
- Keto J et al. Cardiovascular disease risk factors in relation to smoking behaviour and history: a population-based cohort study. Open Heart 2016;3:e000358.
- Prescott R – Smoking and risk of myocardial infarction in women and men; longitudinal population study. BMI 1998;316:1043-1047.
- Greco G et al. Patologia cardiovascolare fumo-correlata. Ital Heart J 2001; 2 (Suppl 1): 37-43.
- Law MR et al – Environmental tobacco smoke esposure and ischaemic heart disease: an evaluation of the evidence. BMJ 1997;315:973-980
- Finucane MM et al – National, regional, and global trends in body-mass index since 1980: systematic analysis of health examination surveys and epidemiological studies with 960 country-years and 9,1 million partecipants. Lancet 2011; 377 (9765): 557-567
- Mechanick JI et al – American Association of Clinical Endocrinologists’ position statement on obesity and obesity medicine Endocr Pract 2012; 18 (5): 642-648
- Sarzani R et al. L’ipertensione arteriosa nel paziente obeso. Raccomandazioni congiunte 2014 della Società Italiana dell’Ipertensione Arteriosa (SIIA) e della Società Italiana dell’Obesità (SIO). raccomandazioni SIIA-SIO.
- Wang TJ et al - Obesity and the Risk of New-Onset Atrial Fibrillation. JAMA. 2004;292(20):2471-2477.
- Loke YK – Association of obstructive sleep apnea with risk of serious cardiovascular events: a systemic review and meta-analysis. Circ cardiovasc Qual Outcomes 2012; 5 (5):720-728
- Wu CY et al. High Blood Pressure and All-Cause and Cardiovascular Disease Mortalities in Community-Dwelling Older Adults. Medicine (Baltimore) . 2015 Nov;94(47):e2160.
- Egan BM et al. Blood Pressure and Cholesterol Control in Hypertensive Hypercholesterolemic Patients: NHANES 1988–2010. Circulation. 2013 July 2; 128(1): 29–41.
- Verdecchia P and Trimarco B. Obesità e ipertensione arteriosa. G Ital Cardiol 2008; 9 (Suppl 1-4): 54S-59S.
- L’alcol e l’assistenza sanitaria primaria. Linee guida cliniche per l’identificazione e l’intervento breve. 2012
- Piepoli MF et al. 2016 European Guidelines on cardiovascular disease prevention in clinical practice. European Heart Journal (2016) 37, 2315–2381
- 2019 ESC/EAS Guidelines for the management of dyslipidaemias:lipid modification to reduce cardiovascular risk - European Heart Journal (2019) 00,1-78.
- Report Diabete in Italia anni 2000-2017. Report Istat del 20 Luglio 2017
- https://www.mayoclinic.org/diseases-conditions/diabetes/symptoms-causes/syc-20371444.
- Cosentino F et al. 2019 ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD. European Heart Journal (2019) 00, 1-69
- Delamater AM – Improving patient adherence. Clin Diabetes 2006; 24; 71-77
- Rossini R et al – Aderenza alla terapia: il fattore di rischio occulto. G It Cardiol 2010; 11 (Suppl 1): 26S-28S.
- Sabatè E – Adherence to Long-Term Therapies: Evidence for Action. Geneva: World Health Organization, 2003.
- Ho PM – Impact of medication therapy discontinuation on mortality after myocardial infarction. Arch Intern Med 2006; 166:1842-1847.
- Holt E, et al. - Sex differences in barriers to antihypertensive medication adherence: findings from the Cohort Study of Medication Ad-herence Among Older Adults (CoSMO). J Am Geri-atr Soc 2013;61:558-64.
- Volpe et al. La terapia con aspirina nella prevenzione cardiovascolare primaria. Documento di consenso intersocietario italiano. G Ital Cardiol 2014;15(7-8):442-451
- American Diabetes Association. 10. Cardiovascular Disease and Risk Management: Standards of Medical Care in Diabetes-2020. Diabetes Care 2020; 43 (Suppl 1): S111-S134.
Fattori psico-sociali ed eventi cardiovascolari
“Nessuna medicina è in grado di curare ciò che la felicità non riesce a curare”- G.G Marquez
La medicina ha sempre cercato di identificare quell’affascinante rete che lega il sentimento alla malattia e tra queste le correlazioni tra mente e cuore “tra l’organo che c’è e l’organo che non c’è” sono di maggior fascino.1
Nel 1942 il Prof. Cannon della Harvard Medical School raccolse, nel suo libro “Vodoo Death” storie su uomini di magia capaci di indurre stati di paura tali da portare alla morte.1
Negli anni 70 Engel raccolse 160 eventi di morte improvvisa collegabili alla presenza di specifici stati emotivi.1
Si rimaneva comunque nell’aneddotica. Solo recentemente, un gruppo di ricerca giapponese attraverso la descrizione di una cardiomiopatia transitoria e reversibile denominata Tako-Tsubo, ha dato dignità scientifica al rapporto mente/ cuore.1
La sindrome tako-tsubo chiamata anche cardiomiopatia da stress, oppure nota come sindrome del cuore infranto è una entità clinica caratterizzata da una disfunzione del ventricolo sinistro, di solito transitoria, che si manifesta con sintomi che possono simulare una sindrome coronarica acuta: dolore toracico, dispnea, alterazioni elettrocardiografiche e alterazioni degli enzimi di necrosi.1,2
La cardiomiopatia takotsubo-like si verifica dopo uno stress psicologico acuto e rappresenta quindi un esempio di lesione neurocardiaca. Sembra probabile che questa drammatica condizione possa essere la punta di un iceberg sotto il quale si annida un problema molto più grande, anche se meno facilmente dimostrabile; vale a dire lesioni neurocardiche che non sono sufficientemente gravi e diffuse da produrre insufficienza cardiaca macroscopica ma che possono predisporre a gravi aritmie cardiache.1 Tale sindrome viene innescata da un trigger emotivo intenso.2
La presentazione clinica è quella dell’infarto del miocardio acuto, spesso correlata da quadro clinico drammatico (15% shock cardiogeno, 23% edema polmonare, 9% TV o FV).2
L’iperincrezione di catecolamine che si genera dall’evento emozionale, crea a livello miocardico una persistente attivazione dei canali del calcio e il conseguente aumento dei livelli intracellulari di tale ione è responsabile dell’innesco della disfunzione ventricolare.2
Numerose evidenze correlano la sindrome depressiva con un aumento dell’incidenza delle malattie cardiovascolari.
La depressione è frequente nel post-infarto e dopo un BPAC: questa condizione aumenta il rischio di morbilità e mortalità.3,4
Uno studio condotto su 374 pazienti ha dimostrato che la depressione maggiore è comune nei pazienti ospedalizzati con insufficienza cardiaca congestizia ed è indipendentemente associata ad una prognosi sfavorevole.5
La depressione maggiore è stata associata ad un aumento sia della mortalità a 3 mesi (odds ratio, 2,5 vs nessuna depressione; P = 0,08) e a 1 anno (odds ratio = 2,23; P = 0,04) che del tasso di ri-ospedalizzazione a 3 mesi (odds ratio = 1,90; p = 0,04) e ad 1 anno (odds ratio, 3,07; P = 0,005). Questi rischi aumentati erano indipendenti dall'età, classe della New York Heart Association, dall’eziologia ischemica di CHF.5
La depressione si associa, inoltre, ad un aumento dell’attivazione piastrinica mediata dalla serotonina e dai farmaci antidepressivi che antagonizzano il recettore piastrinico 5-HT2A.6
Allo stesso modo, la depressione è stata associata a malattie sistemiche che comportano l'induzione di uno stato proinfiammatorio o la sovraregolazione dei marker infiammatori. Ad esempio, è stato riscontrato che i livelli di IL-6 aumentano con l'età e sono associati al benessere cognitivo.
Inoltre, la depressione porta ad un aumento delle lesioni adipose nelle arterie in modelli animali, fornendo un potenziale collegamento tra stress psicologico e malattie vascolari. È stato osservato che lo stress cronico imprevedibile induce una diminuzione dell'attività locomotoria (comportamento di tipo depressivo), oltre a favorire l'aterosclerosi attraverso l'attivazione di vari marker di infiammazione, comprese le proteine C-reattive, IL-6 ed elevate concentrazioni della molecola di adesione delle cellule vascolari 1 e molecola di adesione intercellulare 1 nelle placche e nel plasma di topi knockout per l'apolipoproteina.7
Alti livelli di PCR sono associati con ricorrenze depressive severe. L’infiammazione è coinvolta nella patogenesi dell’aterosclerosi.8
In conclusione, il rapporto tra depressione e danno vascolare può essere meglio compreso in un’ottica integrata di tipo bio-psico-sociale in cui sono implicati l’attivazione neurovegetativa, infiammatoria, immunitaria, i processi emocoagulativi e le risposte comportamentali dell’individuo.
L'ansia e il rischio cardiovascolare
La comorbilità dei disturbi d’ansia con altre patologie determina esiti più sfavorevoli e condiziona il trattamento della patologia associata. L’ansia stimola l’attività del sistema nervoso autonomo che, a sua volta, stimola la produzione di catecolamine, aumentando la frequenza cardiaca e la pressione sanguigna, restringendo le arterie coronariche, e, conseguentemente, aumentando la richiesta cardiaca, l’attività delle piastrine, la coagulazione del sangue e l’infiammazione. A completamento di tale complesso rapporto tra psiche e mente la segnalazione, in uno studio del 2005, i fattori psicosociali (come ansia, stress, ect..) aumentano il rischio di infarto miocardico acuto di 2,67 volte. Allo stesso modo chi soffre di una malattia cardiovascolare ha una maggior prevalenza di malattie a forte connotazione ansiosa come la GAD. Il confronto tra noti fattori di rischio cardiovascolari in termini di rischio relativo è mostrato in Tabella 1.9
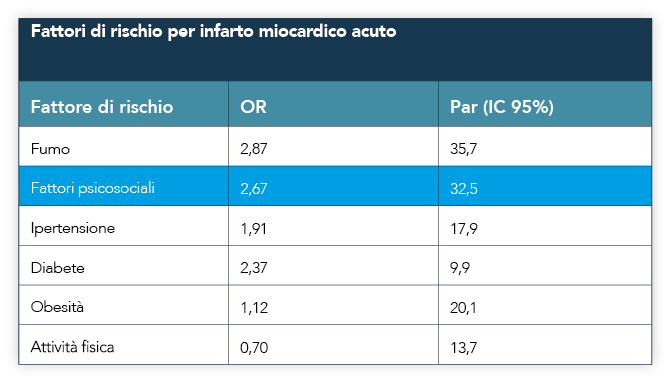
Tabella 1. Tratta da Tabella 7 di ref. 9
L'ansia è una condizione presente nell'ipertensione arteriosa, nella malattia coronarica e negli outcome associati alla chirurgia a cuore aperto. Malgrado quest’associazione risulta alquanto sorprendente tra le condizioni di disturbo d’ansia e le attività cardiovascolari, i legami eziologici e prognostici correlati alla malattia coronarica stanno emergendo solo ora.10
Recenti scoperte scientifiche indicano una forte probabilità che i disturbi d'ansia aumentino il rischio di sviluppare CVD. È stato dimostrato che i disturbi d'ansia sono associati ad un rischio prognostico per eventi avversi cardiovascolari maggiori (MACE: infarto del miocardio [MI], insufficienza ventricolare sinistra, procedura di rivascolarizzazione coronarica e ictus) in pazienti con CVD.10
L'incidenza dei disturbi d'ansia è sostanzialmente maggiore nelle popolazioni CVD rispetto alla popolazione generale.10
Una recente meta-analisi ha dimostrato come il tasso di prevalenza dei disturbi d’ansia in soggetti con CVD è di circa del 16%.10
Il disturbo d'ansia generalizzato e il disturbo da attacchi di panico sono molto più frequenti tra i pazienti con CVD rispetto alla popolazione generale (Tabella 2).10
Prevalenza dei più comuni disturbi d’ansia tra i soggetti con malattia coronarica e nella popolazione generale
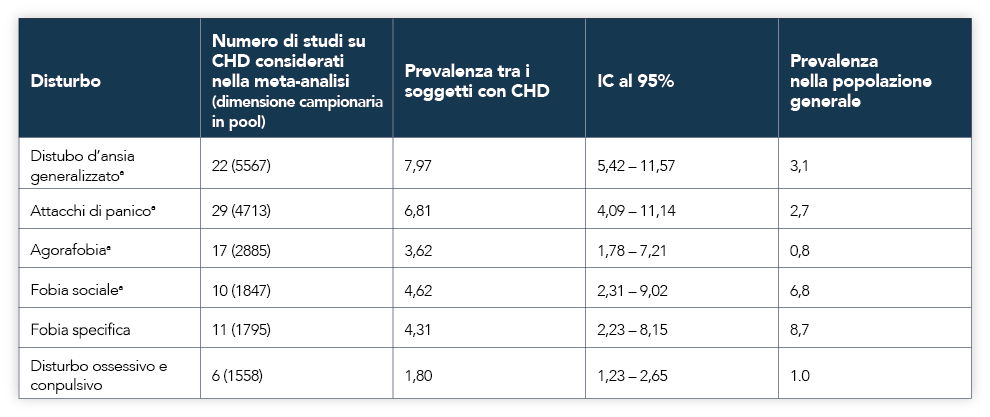
Tabella 2. Tabella 1 di ref. 10
a Maggiore nelle popolazioni con CHD e associato a CVD negli studi eziologici e prognostici.
È importante sottolineare che i disturbi d'ansia sono comuni quanto il disturbo depressivo nella popolazione con sindrome coronarica acuta (ACS) e in seguito ad intervento chirurgico di bypass coronarico. I disturbi d'ansia sono concomitanti con i disturbi depressivi in circa il 50% dei pazienti con CVD, evidenziando una forte comorbilità intra-individuale. Identificare la comorbidità del disturbo d'ansia-depressione è particolarmente importante perché i pazienti con ACS e disturbo d'ansia hanno maggiori probabilità di riportare uno stato depressivo non sufficientemente trattato e di conseguenza un rischio maggiore d’infarto al miocardio.10
Per poter identificare i meccanismi di cardiopatogenesi che potrebbero essere celati in soggetti con disturbi d'ansia, risulta fondamentale distinguere i vari sottotipi di disturbo d'ansia.10
Recenti evidenze scientifiche sottolineano il possibile ruolo dei meccanismi cardiopatogenici biocomportamentali. I fattori comportamentali di panico che possono aumentare il rischio di CVD includono alti tassi di dipendenza da fumo e da nicotina, l'uso di alcol e la mancanza di esercizio fisico attribuita alla paura di esacerbare i sintomi. Studi di monitoraggio suggeriscono lo stato di panico è anche associato a ischemia miocardica, variazioni dell’intervallo QT, flusso coronarico rallentanto, angina microvascolare e rigidità arteriosa.10
Dato che i disturbi d'ansia sono comuni e rappresentano un peso considerevole per la qualità di vita dei pazienti, l'attenzione focalizzata sul trattamento dell'ansia può migliorare il funzionamento quotidiano, ritardare l'insorgenza di CVD e ridurre il carico di morbilità.10
Benzodiazepine e ansia
L’efficacia delle benzodiazepine in risposta a sintomi ansiosi è stata dimostrata dall’ampia letteratura e dall’uso nella pratica clinica degli ultimi 5 decenni. Una delle maggiori indicazioni cliniche delle benzodiazepine riguarda il trattamento dei disturbi d’ansia, soprattutto quando sia necessaria un’azione immediata. La scelta terapeutica di utilizzare le benzodiazepine nel trattamento dei disturbi d’ansia si basa su diversi principi farmacologici ampiamente convalidati: indice terapeutico relativamente elevato, basso rischio di interazioni farmacologiche legate all’induzione enzimatica a livello epatico ed effetti minimi sulle funzioni cardiovascolari ed autonomiche.9
Etizolam nel trattamento dell'ansia
Tra le varie benzodiazepine che vengono utilizzate nel trattamento dell’ansia, un focus particolare merita etizolam, il primo rappresentante di una nuova classe strutturalmente diversa di benzodiazepine, le tienotriazolodiazepine. Pur condividendo un profilo farmacologico simile a quello di altre benzodiazepine, etizolam presenta delle peculiarità: possiede effetti depressivi sul sistema nervoso centrale, quali effetti ansiolitici, anticonvulsivanti, sedativi-ipnotici e miorilassanti. L'etizolam è usato, in alcuni Paesi, nel disturbo d'ansia generalizzato, nel disturbo di panico e per ridurre l'ansia. Vi sono prove del fatto che, oltre ad essere utile nel trattamento del disturbo d'ansia generalizzato, produce un significativo miglioramento dei sintomi depressivi. Una caratteristica insolita del farmaco è il suo effetto sul metabolismo delle monamine.9
Nel cervello di ratto è stato dimostrato come etizolam è in grado di ridurre il turnover della serotonina e di antagonizzare l’aumento di serotonina, noradrenalina e dopamina indotto da stress. Tali peculiarità possono essere d’aiuto in patologie ansiose con componente depressiva come il disturbo d’ansia generlizzato.9
Il profilo cinetico di etizolam suggerisce che l’assorbimento dopo somministrazione orale è rapido con concentrazione plasmatica massima (Cmax) raggiunta entro 0,5-2 ore in tutti i soggetti. L’emivita media di eliminazione (t1/2) è di 3,4 ore. In base alle caratteristiche cinetiche del farmaco e del suo metabolita, l’etizolam può essere considerato come una benzodiazepina a breve durata d’azione.9
Etizolam migliora i disturbi affettivi come ansia e tensione agendo sui recettori delle benzodiazepine dell'ipotalamo e del sistema limbico cerebrale. Etizolam possiede principalmente effetto ansiolitico piuttosto che effetti sedativi.9
Etizolam ha dimostrato anche a dosi terapeutiche elevate, di indurre scarsa sonnolenza (Figura 1).11
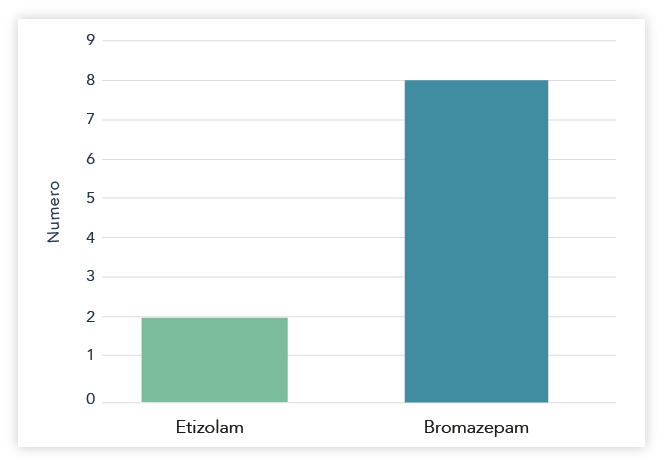
Fig.1 Numero di pazienti con sonnolenza nei primi sette giorni di trattamento con etizolam
(1 mg x 3/die) o con bromazepam (3 mg x 3/die). Figura 10 di ref. 9
In uno studio del 2009 sono stati arruolati un totale di 77 pazienti per valutare le differenze tra gli effetti di etizolam verso placebo sulle prestazioni cognitive. Non vi sono state differenze statisticamente significative.9
Non è stata osservata alcuna tolleranza significativa agli effetti anticonvulsivanti di etizolam. Pertanto, etizolam ha una responsabilità ridotta di indurre tolleranza e dipendenza rispetto alle benzodiazepine classiche. 9
Uno studio del 1989 ha confrontato l'etizolam e l'alprazolam, evidenziando pari efficacia nel trattamento di pazienti affetti da disturbi d'ansia generalizzati con sintomi depressivi lievi come caratteristiche associate. Inoltre, il loro uso è associato a un'eccellente tollerabilità clinica. Vale la pena notare che in questo studio c'era una tendenza dell'etizolam di avere una latenza più breve prima che il suo effetto ansiolitico diventasse evidente e fosse particolarmente efficace nel migliorare i sintomi della somatizzazione dell'ansia rispetto ad alprazolam. Ciò rende etizolam il trattamento preferibile per pazienti selezionati con la somatizzazione dell'ansia (Figura 2).9
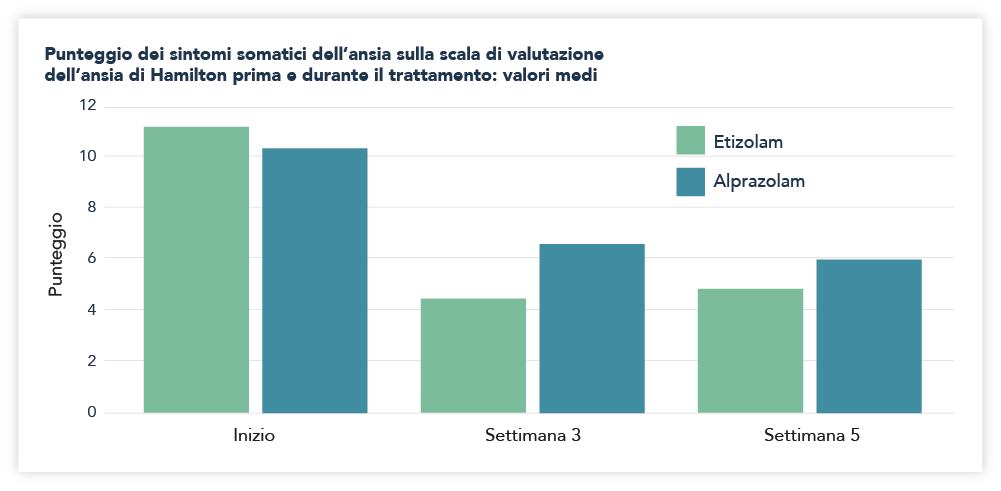
Fig. 2 Confronto sulla Scala di Hamilton tra etizolam e alprazolam. Figura 11 di ref. 9
Etizolam ha un’attività di agonista non completo, quindi con una ridotta propensione alla tolleranza e alla dipendenza, mostrando infatti una particolare affinità per subunità alfa-1 (ansiolitica) rispetto a alfa-2 (sedativa) e alfa-5 (miorilassante). Degno di particolare nota sono gli studi effettuati sulle manifestazioni somatoformi dell’ansia.9
L’efficacia di etizolam nel ridurre l’ansia con basso rischio di indurre fenomeni di tolleranza e di dipendenza, e la scarsa vigilanza, lo rendono un farmaco dal profilo estremamente interessante.11
Etizolam, ad azione medio-breve, viene rapidamente assorbito dall’intestino con scarsa compromissione della vigilanza ma con potente azione ansiolitica, continua a giocare un ruolo centrale nel trattamento dell’ansia.9
Insonnia e rischio cardiovascolare
“Una bella risata e un lungo sonno sono le migliori cure nel libro del medico”. - Proverbio irlandese
Esiste un legame tra i disturbi del sonno e le malattie cardiovascolari.12 Se il sonno avesse un valore di “normalità” come accade per i parametri ematochimici, l’asterisco scatterebbe sotto le 6 ore e sopra le 8 ore al giorno.Una durata stimata di 6-8 ore al giorno del sonno è stata associata ad un rischio di morte e di eventi cardiovascolari inferiore rispetto ad una durata maggiore e inferiore (Figura 3).12
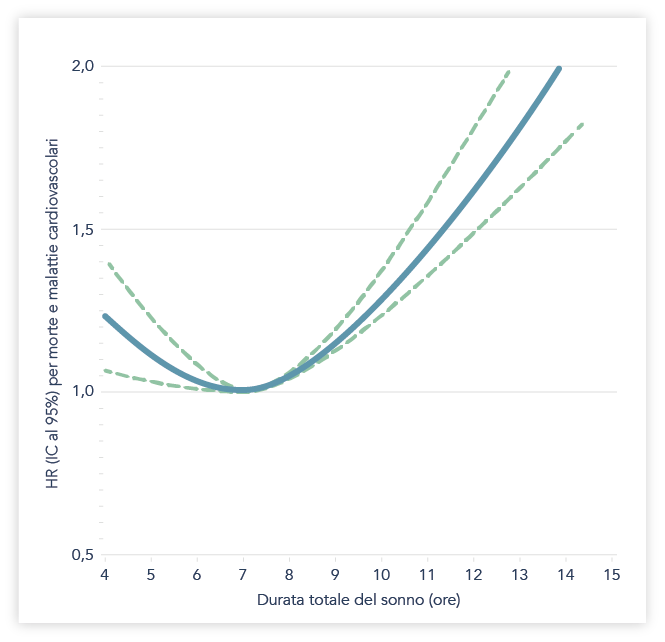
Fig. 3 Curva di spline ristretta all’associazione tra la durata totale di sonno giornaliero e l’insorgenza di malattia cardiovascolari e decessi. L’analisi è stata aggiustata per età, sesso, livello di istruzione, abitudine al fumo, alcolismo, residenza urbana o rurale, regioni geografiche, storia familiare di malattie cardiovascolari (malattia coronarica e ictus), storia di diabete, ipertensione e broncopneumopatia cronica ostruttiva e depressione. Figura 2 di ref. 12
Il ritmo sonno-veglia detta la ciclica variabilità pressoria. Durante la fase di sonno la frequenza cardiaca e la pressione arteriosa si riducono dando luogo al quadro “dipper”. Quando la durata del sonno è di 5-6 ore, il rischio di ipertensione sale di 3,5 volte, sotto le 5 ore di sonno sale ulteriormente a 5,1.9
Con la deprivazione del sonno si vengono ad alterare gli equilibri della funzione del sistema nervoso autonomo, aumento dello stress ossidativo, modifiche delle risposte infiammatorie, metaboliche, coagulative, ormonali e infiammatorie.13-16
La concomitanza temporale di tali modifiche suggerisce la spiegazione del cosiddetto cronorischio17, del perché gli eventi cardiovascolari riconoscono una spiccata variabilità circadiana con un picco mattutino. La deprivazione di sonno aumenta il peso corporeo, il rischio di diabete mellito tipo 2, la pressione arteriosa e modifica in senso pro-aterogeno il rapporto del colesterolo HDL/LDL.15,18,19
Tutto ciò si correla con le basi fisiopatologiche dello sviluppo e della progressione delle malattie cardiovascolari, all’incremento del loro rischio e all’aumento della mortalità totale.20 Un recente studio condotto su un’ampia popolazione di pazienti ha correlato il rischio di IMA con la durata del sonno.21 Gli short sleepers (meno di 6 ore di sonno) presentavano un aumento del rischio del 20% rispetto ai dormitori regolari mentre il long-sleepers (più di 9 ore di sonno) riportavano un rischio aumentato del 34%.21
La spiegazione di tale fenomeno non è chiara: chi dorme meno di 7 ore o più di 8 ore per notte può esporsi ad un rischio cardiovascolare maggiore. Migliorare la qualità del sonno è di fondamentale importanza per ridurre i rischi cardiovascolari.
I disturbi del sonno si correlano non solo a malattie dell’apparato cardiovascolare ma anche ad alcune forme di degenerazione cerebrale di origine vascolare. La valutazione di quanto la deprivazione di sonno influenzi le manifestazioni degenerative di tipo cerebrovascolare mostra come una riduzione del tempo di sonno al di sotto delle 6 ore rappresenti uno specifico fattore di rischio.9
Di seguito alcuni A(P)PUNTI utili per i pazienti:
- Evitare bevande eccitanti la sera
- Evitare pasti eccessivi oppure il digiuno
- Evitare esercizi fisici nelle ore serali
- Evitare attività intellettuali troppo impegnative
- Evitare il fumo prima di coricarsi
- Favorire la regolarità del ciclo sonno-veglia
- Valutare l’uso di farmaci ipnoinducenti
Benzodiazepine e insonnia
La gestione farmacologica dell'insonnia, nella pratica clinica quotidiana, consiste essenzialmente nell'uso delle benzodiazepine. Si tratta di farmaci efficaci, che funzionano "al bisogno", senza cioè alcuna latenza tra la somministrazione e l'insorgenza dell'effetto terapeutico. La migliore conoscenza di questi farmaci consente un uso più razionale, massimizzando i benefici e riducendo i rischi, soprattutto a lungo termine.9
Lormetazepam e insonnia
Il lormetazepam è una benzodiazepina ad azione ipnotica. Un’ampia letteratura ha mostrato e dimostrato, l'efficacia del lormetazepam nella pratica clinica come ipnoinduttore grazie alla grande efficacia nel trattamento dell'insonnia associata alla bassa incidenza di effetti collaterali ed ai limitati effetti residui diurni.9
L'attività sedativa-ipnotica del lormetazepam è 5 volte maggiore di quella del lorazepam, e 10 volte maggiore di quella del diazepam e flurazepam. Lormetazepam si caratterizza per la sua efficacia nel ridurre significativamente il numero dei risvegli notturni, in confronto a zolpidem e placebo, anche in condizioni di rumorosità, chiaro segno di stabilità del sonno indotto (Figura 4).9
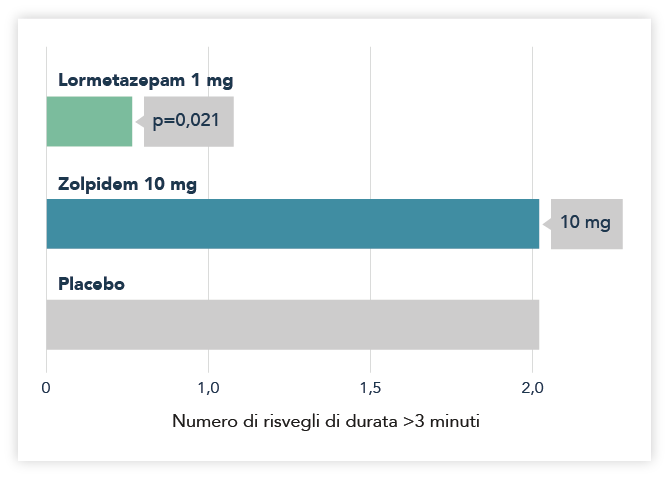
Fig. 4 Numero di risvegli maggiori di 3 minuti per i tre gruppi confrontati. (Modificato da Bosio A. 2003). Figura 13 di ref. 9
Con lormetazepam è stata riscontrata una rapida insorgenza del sonno e una diminuzione del numero di risvegli notturni. La validità dell’effetto ipnotico indotto da lormetazepam è stata valutata anche in termini di sensazione soggettiva manifestata dal paziente. Uno studio controllato condotto per 2 settimane verso placebo ha evidenziato una sensazione di “freschezza” al risveglio sovrapponibile al placebo (Figura 5).9
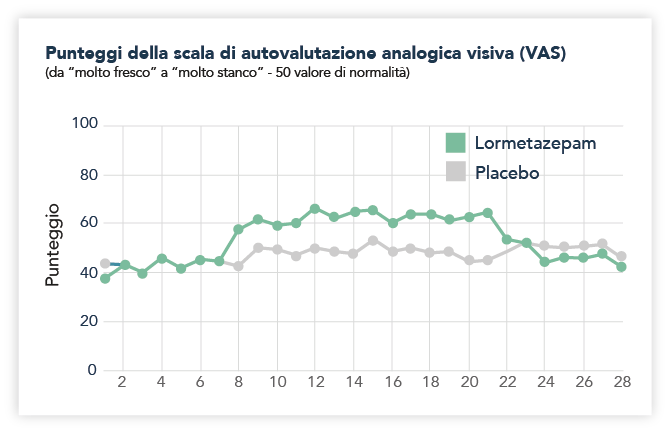
Fig. 5 Confronto tra Placebo e Lormetazepam in termini di “freschezza” al risveglio, misurata secondo una scala di autovalutazione eseguita dai pazienti. Figura 14 di ref. 9
Lormetazepam si caratterizza per la rapidità d’azione che si traduce in un tempo di addormentamento più breve, non solo rispetto al placebo, ma anche ad altri ipnoinducenti come zopiclone (Figura 6).9
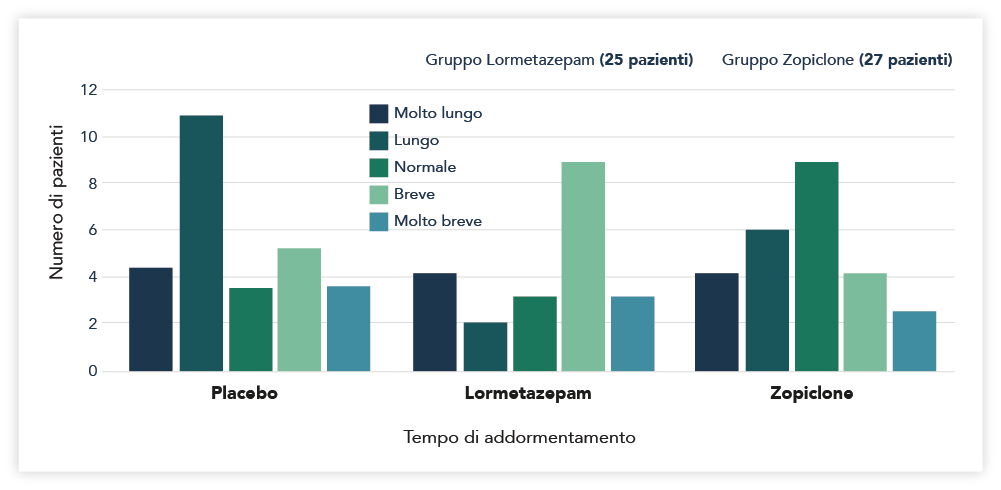
Fig. 6 Tempi di addormentamento con lormetazepam e zopiclone confrontati al placebo. (Modificato da Bosio A. 2003). Figura 15 di ref. 9
Il lormetazepam è impiegato in terapia per migliorare la qualità e la quantità del sonno in pazienti con disturbi del sonno. Le benzodiazepine ipnoinducenti, come il lormetazepam, riducono il tempo di addormentamento e i risvegli notturni ed aumentano le ore di sonno senza effetti di sedazioni importanti al risveglio.9
Il lormetazepam si lega con una maggiore affinità al recettore degli omega 1 (Ki=10 nM) rispetto al recettore degli omega 2 (Ki=29 nM). Pertanto, grazie alla sua azione agonista selettiva e potente sui recettori omega 1 centrali si pensa essere un potente ipnotico con effetti atassici più deboli rispetto ad altre benzodiazepine ad effetto ipnotico. 9
Lormetazepam sembra possedere le caratteristiche di un farmaco ipnotico di scelta in molte condizioni cliniche associate all’insonnia. Ha un rapido assorbimento dopo somministrazione orale, è notevolmente lipofilico, con una durata d’azione ideale per un ipnotico. La selettività recettoriale e i limitati effetti collaterali completano il profilo. 9
BIBLIOGRAFIA
- Samuels MA. The brain-heart connection. Circulation 2007; 116:77-84.
- Ghadri JR et al - International Expert Consensus Document on Takotsubo Syndrome (Part I): Clinical characteristics, diagnostic criteria, and pathophysiology. Eur Heart J 2018;39:2032-46.
- van Melle JP - Prognostic association of depression following myocardial infarction with mortality and cardiovascular events: a meta-analysis. Psychosom Med 2004; 66(6):814-22.
- Lesperance F, Frasure-Smith N et al - Five-year risk of cardiac mortality in relation to initial severity and one-year changes in depression symptoms after myocardial infarction. Circulation 2002; 105: 1049-53.53.
- Jiang W - Relationship of depression to increased risk of mortality and rehospitalization in patients with congestive heart failure – Arch Intern Med 2001; 161: 1849-56.
- Schins A et al - Increased coronary events in depressed cardiovascular patients: 5-HT2A receptor as missing link? Psychosom Med 2003; 65:729:737
- Farooq RK et al. Role of inflammatory cytokines in depression: Focus on interleukin-1β (Review). BIOMEDICAL REPORTS 2017; 6: 15-20.
- Wium-Andersen MK et al. Elevated C-Reactive Protein Levels, Psychological Distress, and Depression in 73131 Individuals. JAMA Psychiatry. 2013;70(2):176-184.
- Mencacci C. Ansia e Insonnia. Il ruolo di Etizolam e Lormetazepam. Clinical Practice 2020.
- Tully PJ et al. Anxiety and Cardiovascular Disease Risk: a Review. Curr Cardiol Rep (2016) 18: 120.
- Bosio A., Terapia farmacologica dell’ansia situazionale. Focus sull’etizolam. European Review for Medical and Pharmacological Sciences Vol. 6 – No 2 (supp. 1) Marzo /Aprile 2002.
- Wang C et al - Association of estimated sleep duration and naps with mortality and cardiovascular events: a study of 116.632 people from 21 countries. Eur Heart J 2019; 40: 1620-1629
- Tobaldini E et al – Sleep, sleep deprivation , autonomic nervous system, and cardiovascular disease. Neurosci Biobehav Rev 2017; 74:321-329
- Grandner MA et al – Sleep duration, cardiovascular disease, and proinflammatory biomarkers .Nat Sci Sleep 2013; 13:93-107
- Cappuccio FP et al – Sleep and cardiometabolic disease. Curr Cardiol Resp 2017; 19:110
- Mullington JM et al – Sleep loss and inflammation. Best Pract Res Clin Endocrinol Metab 2010; 24;141-152
- Thosar SS et al – Role of the circadian system in cardiovascular disease. J Clin Invest 2018; 128:2157-2167
- Jarrin DC et al – Insomnia and hypertension : a systematic review. Sleep Med Rev 2018; 41:3-38
- Vgontzas AN et al. Insomnia with short sleep duration and mortality: the Penn State cohort. Sleep 2010; 33(9): 1159-64.
- Association of longitudinal patterns of habitual sleep duration with risk of cardiovascular events and all-cuse mortality. Wang YH et al – JAMA Network open 2020; 3 (5) e205246 . doi 10.1001 /jamanetworkopen.2020.5246.
- Daghlas I et al – Sleep duration and myocardial infarction. J Am Coll Cardiol 2019: 74:1304-1314.
Commenti
Lascia un commento:

Clinical Practice è un sito del network XGATE
XGate è un sistema di registrazione centralizzato che permette di accedere con le stesse credenziali (Email e password) a tutti i siti e app realizzati da Axenso



